酸化物の構造|セラミックス技術コラム
セラミックス技術コラム
酸化物の構造

単一酸化物
酸素はクラーク数は1、地殻で49.5%をしめる元素で、しかもフッ素についで電気陰性度が大きいため多くの金属元素と酸化物をつくり、資源的に広く利用されている。単一酸化物(Simple oxide)の一般的な形としてはR2O, RO, R2O3, RO2などがあるが、これらの単一格子はR2O3をのぞいてすべて既述の構造型に属する。
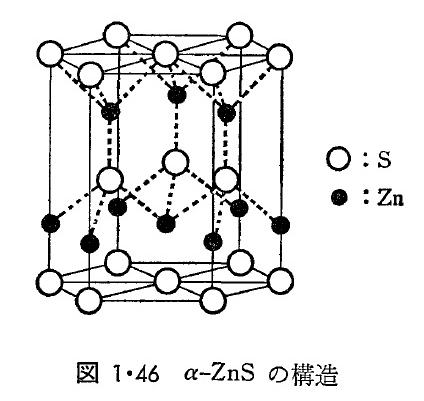
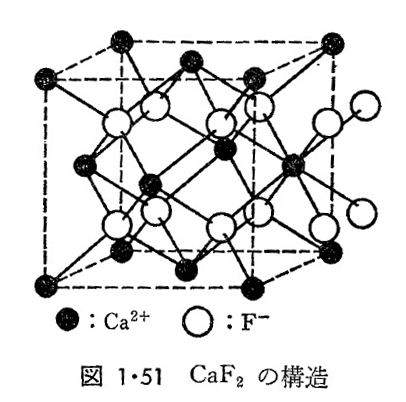
まず、R2OとしてはLi2O, Na2O, K2Oなどのアルカリ金属の酸化物があるが、いずれもCaF2構造(図1・51)の変形である。すなわち、この構造のCaの位置にOを、Fの位置にRをおき、逆CaF2構造(anti-fluorite sturucture)とよんでいる。つぎに、ROの大部分は、MX6配位のNaCl構造(図1・46)をとるものにBeO, ZnOがある。
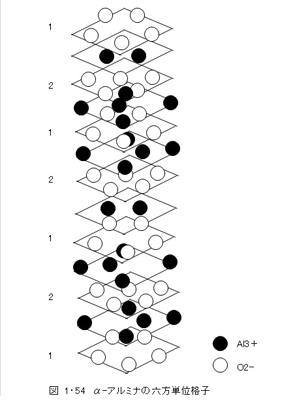
R2O3の代表的結晶はα-アルミナ(α-alimina, α-Al2O3)である。これは菱面体格子であるが、換算して図1・54のような六方格子で示したほうが、配列をよく理解できる。O2- は六方細密充てん(1-2-1-2-1-2)に配列し、その層間のすき間の2/3をAl3+がしめている。
層間にはいったAl3+はMX6の八面体形結合を形成しているが、Al3O3のイオン半径比は0.30でMX6の条件0.414よりも小さいので、八面体は多少ひずみ菱面対格子となるのである。
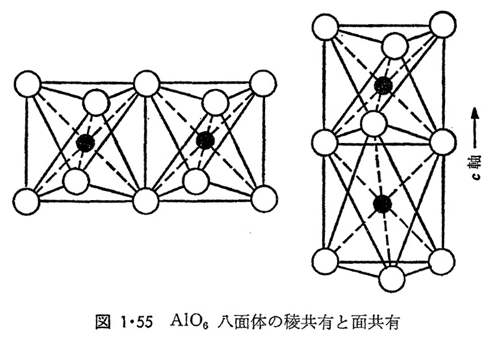
構造内のAlO6八面体は図1・55にみられるようにc軸方向に面共有、c軸に直角の3方向に稜共有の組み合わせで構成され、これがα-アルミナがダイヤモンドにつぐ硬さをもつ原因となっている。
さきの表1・5においてα-アルミナのMadelung定数が最大であったことに注意せよ。α-Al2O3のほかに、α-Fe2O3、Cr2O3、Ti2O3、V2O3などがこれに属する。

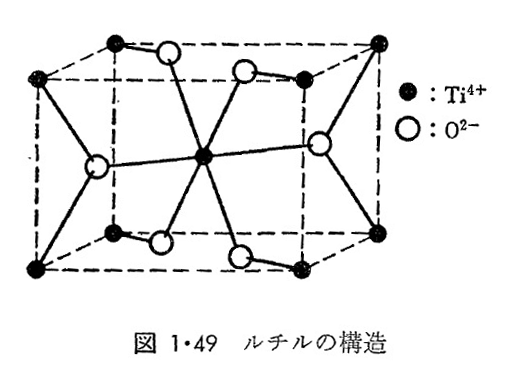
最後のRO2では、代表的な例として、MX8配位のCaF2構造とMX6配位のルチル構造(図1・49)があり、特異な例として供給結合性の強いMX4配位のSiO2がある。イオン半径比が0.73以上ではCaF2型としてThO2、CeO2、HfO2、UO2など、ルチル型としてTiO2、SnO2、MnO2、VO2、MoO2、PbO2などがある。
新版 セラミックスの材料化学
荒井康夫 著
お問い合わせ
特注サイズや形状も、1点から承ります。
お気軽にお問い合わせください。
-
アスザック株式会社
ファインセラミックス事業部受付時間:9:00~17:00(土日祝休み)
FAX : 026-251-2160